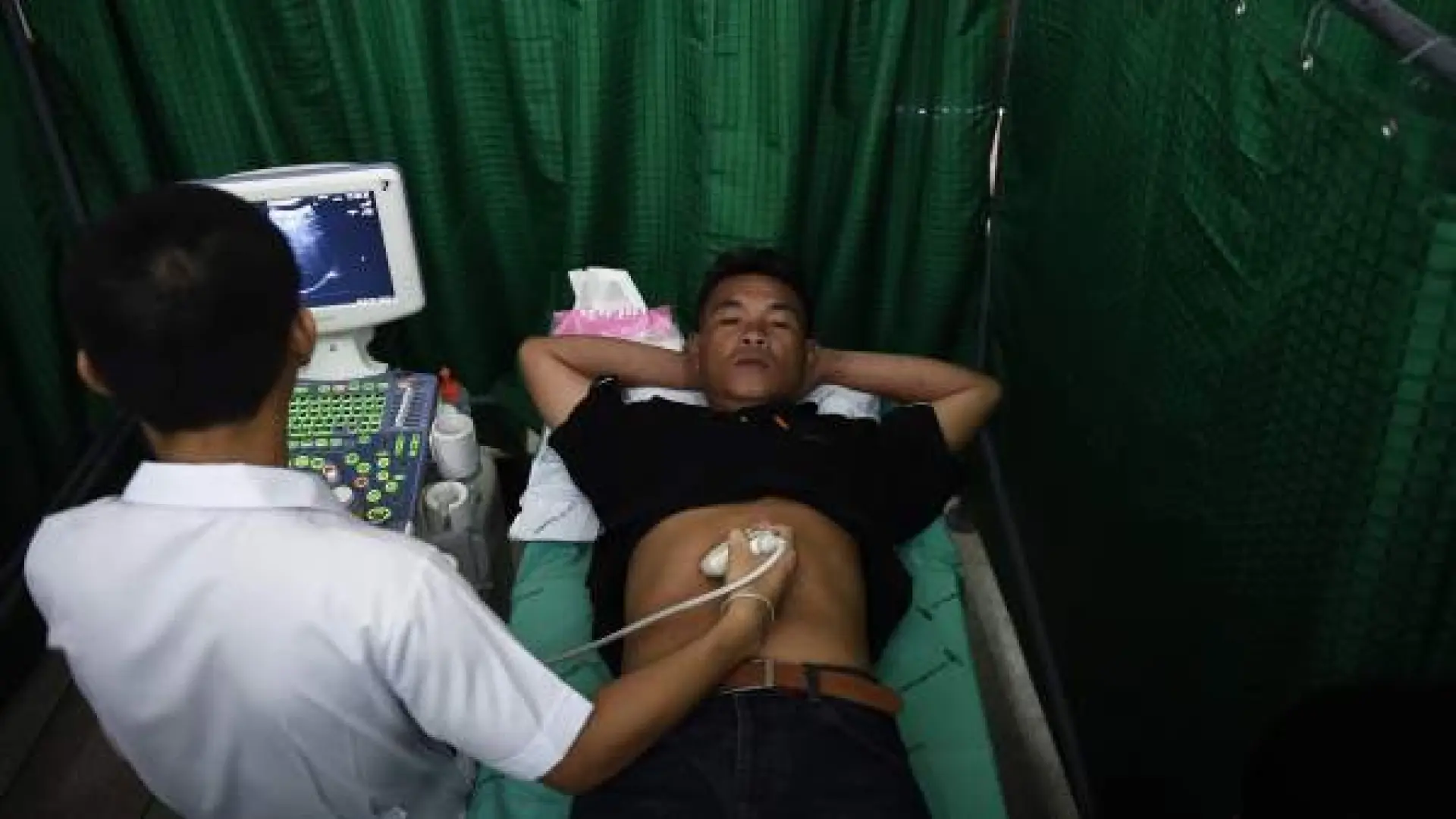
Uno de los mayores factores de riesgo para desarrollar cáncer de hígado es una dieta rica en grasas, pues reconfigura las células hepáticas y las hace más propensas a ser cancerígenas.
Así se desprende de un estudio dirigido por investigadores del Instituto Tecnológico de Massachusetts (MIT, por sus siglas en inglés) y publicado en la revista 'Cell'. Los investigadores descubrieron que, en respuesta a una dieta rica en grasas, los hepatocitos maduros del hígado revierten a un estado inmaduro, similar al de las células madre. Esto les ayuda a sobrevivir a las condiciones estresantes creadas por la dieta rica en grasas, pero a largo plazo aumenta su probabilidad de desarrollar cancer.
«Si las células se ven obligadas a lidiar con un factor estresantecomo una dieta alta en grasasuna y otra vez, harán cosas que las ayudarán a sobrevivir, pero con el riesgo de aumentar la susceptibilidad a la tumorigénesis», explica Alex K. Shalek, director del Instituto de Ingeniería Médica y Ciencias, y miembro del Instituto Koch para la Investigación Integral del Cáncer en el MIT.
Los investigadores también identifican varios factores de transcripción que parecen controlar esta reversión y creen que podrían ser buenos objetivos para medicamentos que ayuden a prevenir el desarrollo de tumores en pacientes de alto riesgo.
Reversión celular
Una dieta rica en grasas puede provocar inflamación y acumulación grasa en el hígadouna afección conocida como enfermedad hepática esteatósica, la cual, que también se origina por diversos tensiones metabólicas a largo plazo -como el consumo excesivo de alcohol-puede provocar cirrosis hepática, insuficiencia hepática y, finalmente, cáncer.
En el nuevo estudio, los investigadores querían descubrir qué sucede exactamente en las celulas del higado cuando se exponen a una dieta rica en grasas; en particular, qué genes se activan o desactivan a medida que el hígado responde a este estrés a largo plazo.
Para ello, alimentaron a ratones con una dieta rica en grasas y realizaron la secuenciación de ARN unicelular de sus células hepáticas en momentos clave a medida que progresaba la enfermedad hepática. Esto les permitió monitorear los cambios en la expresión génica que se produce a medida que los ratones progresan desde la inflamación hepática hasta la cicatrización tisular y, finalmente, el cáncer.
En las primeras etapas de esta progresióndescubrieron que la dieta rica en grasas indujo a los hepatocitos -el tipo celular más abundante en el hígado- a activar genes que les ayudan a sobrevivir al entorno estresante. Estos incluyen genes que los hacen más resistentes a la apoptosis y más propensos a proliferar.
Mutación
Al mismo tiempo, esas células comenzaron a desactivar algunos de los genes que son críticos para el funcionamiento normal de los hepatocitos, incluidas las enzimas metabólicas y las proteínas secretadas. Algunos de esos cambios se producen de inmediato, mientras que otros, como la disminución de la producción de enzimas metabólicas, Llegaron de forma más gradual a lo largo de un período más prolongado. Casi todos los ratones con una dieta rica en grasas acabaron desarrollado cáncer de hígado al final del estudio.
Cuando las celulas están en un estado más inmaduroparece que tienen más probabilidades de volverse cancerosas si se produce una mutación más adelante, según los investigadores. «Estas células ya han activado los mismos genes que necesitarán para volverse cancerosas. Ya se han alejado de la identidad madura que, de otro modo, reduciría su capacidad de proliferación», afirma Constantine Tzouanas, estudiante de posgrado del MIT, quien añade: «Una vez que una célula detecta la mutación incorrecta, se dispara y ya se ha adelantado en algunas de las características distintivas del cáncer».
Proceso de 20 años
Tras identificar estos cambios en ratones, los investigadores quisieron descubrir si algo similar podría ocurrir en personas con enfermedades hepáticas. Para ello, analizaron datos de muestras de tejido hepático extraído de pacientes en diferentes etapas de la enfermedad. También analizaron tejido de personas con enfermedad hepática, pero que aún no habían desarrollado cáncer.
Estos estudios revelaron un patrón similar al observado en ratones: la expresión de genes necesarios para la función hepática normal disminuyó con el tiempo, mientras que la de genes asociados con estados inmaduros aumentado. Además, los investigadores descubrieron que pudieron predecir con precision la supervivencia de los pacientes evaluarán en un análisis de sus patrones de expresión génica.
«Los pacientes con mayor expresión de estos genes pro-supervivencia celular, que se activa con una dieta rica en grasassobrevivieron menos tiempo después del desarrollo de los tumores», recalca Tzouanas, antes de agregar: «Y si un paciente presenta menor expresión de genes que apoyan las funciones que el hígado realiza normalmente, también sobrevive menos tiempo».
Si bien los ratones de este estudio desarrollaron cáncer en aproximadamente un año, los investigadores calculan que el proceso probablemente se extenderá por un período más largo en humanos, alrededor de 20 años. esto varía según la dieta de cada individuo y otros factores de riesgo, como el consumo de alcohol o las infecciones virales, que también pueden promover la reversión de las células hepáticas a un estado inmaduro.